Розділ 1. Обґрунтування вибору біологічного агента

Найздібнішими до боротьби із забруднювачами різного типу є представники роду Pseudomonas. Клітини цих мікроорганізмів містять оксидоредуктази і гідроксилази, здатні розкладати велике число молекул вуглеводнів та ароматичних сполук, таких як бензол, ксилол, толуол. Гени, що кодують ці ферменти, знаходяться в складі плазмід. Наприклад, плазміда ОСТ відповідає за розкладання октану і гексану, XYL… Читати ще >
Розділ 1. Обґрунтування вибору біологічного агента (реферат, курсова, диплом, контрольна)
Екологічні аспекти вибору біологічного агента
Поліциклічні ароматичні вуглеводні (ПАВ) є пріоритетними забруднювачами внаслідок повсюдного поширення і негативного впливу на живі організми. ПАВ входять до складу важких фракцій нафти (близько 5−10%) і потрапляють у навколишнє середовище в результаті аварійних розливів нафтопродуктів, транспортування і при переробці нафти. Велика кількість ПАВ утворюється при неповному згорянні органічних сполук і постійно присутня у викидах ТЕЦ, коксо-, газо — та нафтохімічних виробництв [6].
Продукти на основі нафти є основним джерелом енергії для промисловості і повсякденного життя, що зумовлює постійний розвиток та зростання обсягів нафтопереробної галузі. В свою чергу, така ситуація спричинила суттєве забруднення води і ґрунту вуглеводнями різного походження. Технології, що використовуються сьогодні для вирішення цієї проблеми, є дорогими і не можуть призвести до повного очищення, а також призводять до появи ряду побічних продуктів.
Процес біологічного очищення визначається як використання мікроорганізмів для детоксикації або видалення забруднюючих речовин за рахунок їх метаболічних можливостей. Він є перспективним способом видалення і деградації багатьох забруднювачів навколишнього середовища, включаючи продукти нафтової промисловості. Крім того, технологія біологічного очищення, як вважають, є неінвазивним і відносно економічним способом. Успіх біоремедіації залежить від здатності створювати і підтримувати умови, які сприяють біодеградації у навколишньому середовищі. Однією з важливих вимог є наявність мікроорганізмів з відповідною метаболічною здатністю. Якщо ці мікроорганізми присутні, то їх можливість росту на вуглеводневому середовищі залежить від комбінації двох чинників: біохімічної взаємодоповнюваності організмів і стійкості до токсичної дії вуглеводнів. Очевидно, ці два чинники мають бути оптимальними. Враховуючи характер багатокомпонентних нафтових забруднень, мікроорганізми (асоціації мікроорганізмів) повинні мати можливість рости на більшості компонентів забруднюючих речовин і бути стійкими до токсичної дії для повної мінералізації нафтопродуктів.
Оптимальні темпи росту мікроорганізмів і біодеградації вуглеводнів можливо досягти шляхом забезпечення оптимальних концентрацій поживних речовин і кисню, рН та температури. Фізичні та хімічні характеристики нафтопродуктів, площа поверхні розділу фаз також є важливими детермінантами успіху біологічного очищення. Існують два основні підходи до біологічного очищення розливів нафти:
a) біоаугментація, коли відомі нафтоокиснюючі бактерії додаються до існуючих природних мікробних популяцій екосистеми, де стався розлив;
б) біостимуляції, коли ріст нативних деструкторів нафти стимулюється додаванням поживних речовин або інших субстратів для забезпечення оптимальних умов життєдіяльності мікроорганізмів [3].
Все частіше забруднення навколишнього середовища носить комплексний характер, обумовлений як присутністю органічних токсикантів, так і сполук важких металів. Наявність високих концентрацій важких металів у ґрунтах значно знижує швидкість деградації органічних забруднювачів і, нагромаджуючись у сільськогосподарських рослинах, дані сполуки можуть надходити в організм людини і викликати ряд важких захворювань.
Найздібнішими до боротьби із забруднювачами різного типу є представники роду Pseudomonas. Клітини цих мікроорганізмів містять оксидоредуктази і гідроксилази, здатні розкладати велике число молекул вуглеводнів та ароматичних сполук, таких як бензол, ксилол, толуол. Гени, що кодують ці ферменти, знаходяться в складі плазмід. Наприклад, плазміда ОСТ відповідає за розкладання октану і гексану, XYL — ксилолу і толуолу, NAH — нафталіну, CAM — камфори. Плазміди САМ і NAH забезпечують власне перенесення, індукуючи схрещування бактеріальних клітин; інші плазміди можуть бути перенесені тільки в тому випадку, якщо в бактерії введені інші плазміди, що забезпечують схрещування [8].
Ці мікроорганізми зручно використовувати для очищення нафтових плям на суші або морі при різних аваріях. Для більшої ефективності створюють мікроемульсію, що містить бактеріальні штами і капсули з сумішшю основних поживних елементів — азоту, фосфору і калію всередині. Додавання цих речовин стимулює розмноження бактеріальних штамів. Застосування такого методу дозволяє очистити від 70 до 90% забрудненої поверхні, за цей же час очищується всього близько 10−20% необробленої поверхні.
Перевага бактеріального очищення в порівнянні з хімічним в тому, що вона не викликає появи нового забруднюючого агента в навколишньому середовищі. Щільність фітопланктону після бактеріального очищення підвищується. Деякі мікроорганізми здатні змінювати молекулу ксенобіотика і робити її доступною і привабливою для інших мікроорганізмів («кометаболізм»). Прикладом може служити розкладання інсектициду паратіона під дією двох штамів Pseudomonas — P. aeruginosa і P. stuzeri. У деяких випадках відбувається неповне перетворення молекули ксенобіотика — фосфорилювання, метилювання, ацетилювання, тощо, результатом якого є втрата цією речовиною токсичності [5].
Штам Pseudomonas aureofaciens BKM B-2501 використовується для біодеградації (утилізації) ПАВ в умовах забруднення ґрунтів солями нікелю.
Фітостимулюючі властивості штаму є дуже важливими при проведенні фіторемедіаційних технологій, заснованих на використанні рослин і асоційованих з рослиною мікроорганізмів для очищення навколишнього середовища.
Технічним ефектом, який може бути отриманий при використанні даного штаму, є швидка деградація ПАВ в ґрунтах при їх забрудненні солями нікелю, а також захист рослин від токсичного впливу ПАВ і поліпшення їхнього росту при культивуванні внаслідок зменшення вмісту ПАВ у цих ґрунтах за рахунок біодеградації [14].
Вихідним бактеріальним штамом для отримання даного плазмідного штаму є штам Pseudomonas aureofaciens BS1393, який пригнічує ріст багатьох фітопатогенних грибів і бактерій за рахунок продукування антибіотико-активних сполучень. Діюча речовина — живі бактеріальні клітини, які колонізують листя і стебла рослин. На основі цього штаму розроблений біопрепарат Псевдобактерин-2 (ПС-2): культуральна рідина з концентрацією живих клітин 6−8Ч1010 в мл і паста — 3−4Ч1013 живих клітин в 1 грамі [21].
Захисна дія базується на здатності клітин бактерій продукувати позаклітинні метаболіти (сидерофори, феназини), які пригнічують ріст фітопатогенних бактерій і грибів, а також підвищують власний імунітет рослини. Крім того, клітини бактерій синтезують індоліл-3-оцтову кислоту (ІОК, стимулятор росту) і різноманітні органічні кислоти, які перетворюють нерозчинні фосфати ґрунту в доступні для рослин форми, а також продукують різноманітні фітогормони [21].
При отриманні плазмідних штамів PGPR Pseudomonas — P. aureofaciens BS 1393 (pB217,pB501) необхідно враховувати можливий негативний вплив плазмід на фітостимулюючі і захисні властивості штамів. В отриманих штамах наявність плазмід біодеградації нафталіну і стійкості до важких металів не зменшувало продукування феназинових антибіотиків (рис. 1.1) [22].
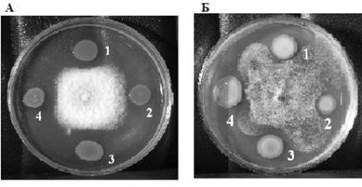
Рис. 1.1. Антагоністична активність плазмідних штамів P. aureofaciens BS1393 in vitro: А — пригнічення росту F. graminearum, Б — R. solani. 1 — P. aureofaciens BS1393, 2 — P. aureofaciens BS1393(pBS216,pBS501), 3 — P. aureofaciens BS1393(pOV17), 4 — P. aureofaciens BS1393(pBS216)
Антагоністична активність запропонованого штаму Pseudomonas aureofaciens ВКМ В 2501 по відношенню до фітопатогенних грибів і бактерій не відрізняється від активності вихідного безплазмідного штаму P. aureofaciens BS1393 [14].
Здатність ризосферних бактерій до синтезу фітогормонів може позитивно вплинути на ефективність фіторемедіації за рахунок збільшення вегетативної маси рослин. Всі штами-деструктори синтезують індоліл-3-оцтову кислоту в кількості 2−6 мкг/мг сухих клітин (рис. 1.2).

Рис. 1.2. Вплив різних варіантів штаму P. aureofaciens BS1393 на ріст пшениці в присутності нафталіну (200 мкг/г)
Штам бактерій Pseudomonas aureofaciens BKM В-2501 містить природну плазміду біодеградації нафталіну pBS216 та природну плазміду pBS501, що містить cnr-подібний оперон, який забезпечує стійкість до кобальту і нікелю, пов’язану з вилученням катіонів металів з клітини [18].
При використанні плазмідних штамів в ремедіації ґрунтів велике значення має стабільність підтримання плазмід і збереження фенотипу інтродукуючих мікроорганізмів. Порівняння стабільності плазмід у одного і того ж варіанта штаму показало, що на середовищі М 9, зазвичай, стабільність вища ніж на LB. Це може бути пов`язано з більш тривалим часом генерації штамів на бідних середовищах. Для P. aureofaciens BKM В-2501 час однієї генерації в експоненційній фазі росту на середовищі LB склало приблизно 40 хв, а на М 9 з гліцерином — 1,5 год. Окрім стабільності підтримання, важливою характеристикою плазмід є їх структурна стабільність. Низька швидкість росту і накопичення продуктів неповного окиснення нафталіну може бути результатом нездатності плазмідних генів катаболізму нафталіну ефективно здійснювати експресію в результаті структурних змін плазміди, які відбуваються під час її перенесення в даний штам [22].
Штам бактерій Pseudomonas aureofaciens BKM В-2501 стійкий до катіонів нікелю та кобальту. Максимальна толерантна концентрація (МТК) хлориду нікелю — 400 мкМ, хлориду кобальту — 200 мкМ. Рівень резистентності до нікелю і кобальту у пропонованого штаму P. aureofaciens BKM В-2501 в 4 рази вище, ніж у чутливого варіанта P. aureofaciens BS1393(pBS216), незалежно від джерела вуглецю в середовищі вирощування (глюкоза або нафталін). Нікель не мав негативного впливу на життєздатність стійкого штаму PCL1391(pBS216,pBS501) — Pseudomonas aureofaciens BKM В-2501. Як в контролі, так і в присутності металу при однаковій густині культури кількість КУО співпадала і зростала. В кінці експоненційного росту титр клітин склав 1,2Ч1010 КУО/мл порівняно з початковим значенням 1,5Ч107 КУО/мл.
У присутності 100 мкМ нікелю чутливий штам бактерій P.aureofaciens BS1393(pBS216) за 36 годин окисляє близько 11% нафталіну. У присутності нікелю пропонований штам P. aureofaciens ВКМ В-2501 за 21 годину окисляє близько 98% нафталіну, стільки ж, скільки чутливий штам P. aureofaciens BS1393(pBS216), вирощений без додавання металу [14].
Збереження активності ферментів біодеградації нафталіну у пропонованого штаму при різних умовах культивування (наявність або відсутність іонів нікелю) свідчить про здатність даного штаму ефективно деградувати ПАВ в присутності хлориду нікелю.
Питома активність ключових ферментів біодеградації нафталіну, а саме, нафталін диоксигенази, саліцилат гідроксилази і катехол-1,2-диоксигенази в присутності хлориду нікелю (100 мкМ) у пропонованого штаму P. aureofaciens BKM В-2501 у 6, 9 і 8 разів вище, ніж у чутливого P. aureofaciens BS1393(pBS216) [14].
Таблиця 1.1. Питома активність ключових ферментів біодеградації нафталіну (нмоль/хв мг білка) у різних варіантів штаму P. сhlororaphis PCL1391.