Роль порушень судинної регуляції у виникненні перинатальних ускладнень у вагітних високого ризику

Содержание L-аргинина в крови определяли с помощью фотометрического метода, в основу которого положена реакция L-нафтола с гипобромидным реактивом. Уровень гомоцистеина определялся методом ферментативной циклической реакции, с помощью набора Diasyis (Германия) с использованием анализатора «Respons 920» (Германия) по методике производителя. Для количественного определения плацентарного фактора… Читати ще >
Роль порушень судинної регуляції у виникненні перинатальних ускладнень у вагітних високого ризику (реферат, курсова, диплом, контрольна)
Мета встановити роль порушень судинної регуляції у виникненні перинатальних ускладнень у вагітних високого ризику.
Пацієнти та методи. Обстежено 50 вагітних жінок після допоміжних репродуктивних технологій із гепатобіліарними порушеннями (основна група), 50 вагітних жінок після допоміжних репродуктивних технологій без таких порушень (група порівняння) і 50 соматично здорових жінок із неіндукованою вагітністю (контрольна група) у терміні гестації 14−16 тижнів. Вміст L-аргініну в крові визначено за допомогою фотометричного методу, в основу якого покладено реакцію L-нафтола з гіпобромідним реактивом. Рівень гомоцистеїну визначено методом ферментативної циклічної реакції, за допомогою набору Diasyis (Німеччина) з використанням аналізатора Respons 920 (Німеччина) за методикою виробника. Для кількісного визначення плацентарного фактора росту людини (PLGF) в зразках плазми крові використано імунохімічний метод з електрохемілюмінесцентною детекцією (ECLIA).
Результати. Для визначення ролі порушень регуляції судинного гомеостазу у виникненні ускладнень вагітності при печінкових порушеннях в основній групі виділено 2 підгрупи: 1-ша 9 жінок із суттєвими акушерськими й перинатальними порушеннями (викидні та завмерлі вагітності, прееклампсія тяжкого ступеня, декомпенсований дистрес плода), 2-га 31 жінка без таких порушень. Встановлено, що вагітність після програм допоміжних репродуктивних технологій проходила з особливо тяжкими ускладненнями в тих жінок із гепатобіліарними порушеннями, в яких вже на початку вагітності формування і розвиток плаценти відбувались в умовах ендотеліальної дисфункції (зниження рівня L-аргініну до 39,8±2,0 проти 45,8±1,6 ммоль/л у жінок без суттєвих порушень гестаційного процесу, p<0,05), негативної дії гомоцистеїну (підвищення до 7,4±0,44 проти 6,4±0,36 мкмоль/л, p<0,05), порушень процесів ангіогенезу (зниження рівня PIGF крові 70,5±11,9 проти 103,7±9,8 пг/мл, p<0,05). Отже, ці фактори можуть бути ранніми прогностичними маркерами тяжких акушерських і перинатальних порушень при індукованій вагітності в жінок із гепатобіліарними порушеннями. Висновки. В умовах гомеостатичного дисбалансу в даної категорії жінок порушення ендотелію та факторів судинної регуляції лежать в основі патогенезу репродуктивних, акушерських і перинатальних ускладнень, що є теоретичною передумовою для розробки патогенетично обґрунтованого комплексу профілактики й лікування, спрямованого на корекцію виявлених порушень.
Ключові слова: вагітність, допоміжні репродуктивні технології, печінка, акушерські ускладнення, ендотелій.
Значущість проблеми перинатальних наслідків лікування безпліддя зростає, що обумовлено, з одного боку, незмінно високою часткою безплідних пар у популяції, а з іншого — все більшим поширенням допоміжних репродуктивних технологій (ДРТ) [1]. За різними даними, вагітність, яка настала в результаті застосування ДРТ, відноситься до категорії високого ризику і відрізняється підвищеною частотою мимовільного переривання та акушерських ускладнень [12].
Проблема «патологія печінки і вагітність» також постійно перебуває в полі зору акушерів-гінекологів, а постійно зростаюче негативне навантаження різних факторів на організм жінки призводить до зростання частоти патологічних станів печінки, що, своєю чергою, ускладнює перебіг вагітності й погіршує її перинатальні наслідки [2, 11, 13].
Як відомо, ендотеліальна дисфункція є універсальним патогенетичним механізмом більшості захворювань, ендотелій не тільки регулює судинний тонус, але й бере участь у процесах атерогенезу, тромбоутворення, захисту цілісності судинної стінки. Крім того, ендотелій виробляє велику кількість біологічно активних речовин, які впливають на тонус та ангіогенез судин, регулюють гемостаз, адгезію і агрегацію тромбоцитів, імунну та протизапальну відповідь [8].
При захворюваннях печінки відбувається пошкодження ендотеліальних клітин печінкових синусоїдів, зміни внутрішньопечінкової гемодинаміки, збільшення продукції цитокінів і вільних радикалів [3]. Процеси ангіогенезу в печінці тісно пов’язані з функціональною спроможністю ендотелію. Оксид азоту (NO) синтезується гепатоцитами й клітинами ретикулоендотеліальної системи печінки [10]. При хронічних процесах у печінці пригнічуються процеси біосинтезу NO, унаслідок чого порушується баланс між вазоконстрикторами і вазодилататорами [13].
Ендотеліальна дисфункція відіграє важливу роль і при розладах репродуктивної сфери, зокрема безплідді, звичному невиношуванні вагітності [4, 7]. Деякі автори навіть вважають її основою патогенезу таких станів.
Серед численних факторів ендотеліального походження визнаним маркером ендотеліальної дисфункції є NO. Оксид азоту утворюється з L-аргініну під дією ферменту NO-синтази (NOS). Саме системі L-аргінін — NO сучасне акушерство відводить провідну вазорегуляторну роль у період гестації [5, 14].
Особливе значення для розвитку судинної мережі плаценти та її нормального функціонування мають судинні фактори, що стимулюють проліферацію ендотеліальних клітин і підвищують їх життєздатність, до яких відноситься ендотеліальний фактор росту (VEGF), плацентарний фактор росту (PlGF) і фактор росту фібробластів (bFGF) [13].
Важливим фактором репродуктивних та акушерських порушень є гіпергомоцистеїнемія, яка призводить до пошкодження та активації ендотеліальних клітин, що значно підвищує ризик розвитку тромбозів. З іншого боку, гіпергомоцистеїнемія може супроводжуватися розвитком вторинних аутоімунних реакцій і сьогодні розглядається як одна з причин АФС. Гомоцистеїн індукує апоптоз клітин трофобласту і значно знижує вироблення хоріонічного гонадотропіну, що може бути причиною розвитку акушерських ускладнень, пов’язаних із порушенням імплантації [6].
З урахуванням сучасних уявлень про ендотеліальну дисфунцію як універсальний пусковий механізм репродуктивних порушень, ролі судинних змін у порушенні процесів плацентації, а також виявленої нами в жінок із безпліддям і гепатобіліарними порушеннями генетичної схильності до ендотеліальної дисфунції (несприятливі варіанти поліморфізмів гену eNOS) [13], нами проведено дослідження в таких жінок рівня донатора NO — L-аргініну, фактора пошкоджуючого ендотелій — гомоцистеїну та фактора ангіогенезу — PlGF.
Мета роботи — встановити роль порушень судинної регуляції у виникненні перинатальних ускладнень у вагітних високого ризику.
Матеріали та методи дослідження Для оцінки стану судинної регуляції у вагітних жінок високого ризику (вагітність після ДРТ, функціональні порушення печінки), залежно від розвитку акушерських і перинатальних ускладнень, проведено дослідження відповідних показників у 50 вагітних жінок після ДРТ із гепатобіліарними порушеннями (основна група), у 50 вагітних жінок після ДРТ без таких порушень (група порівняння), у 50 соматично здорових жінок із неіндукованою вагітністю (контрольна група) в терміні вагітності 14−16 тижнів.
Вміст L-аргініну в крові визначено за допомогою фотометричного метода, в основу якого покладено реакцію L-нафтола з гіпобромідним реактивом. Рівень гомоцистеїну визначено методом ферментативної циклічної реакції, за допомогою набору Diasyis (Німеччина) з використанням аналізатора Respons 920 (Німеччина) за методикою виробника. Для кількісного визначення плацентарного фактора росту людини (PLGF) в зразках плазми крові використано імунохімічний метод з електрохемілюмінесцентною детекцією (ECLIA).
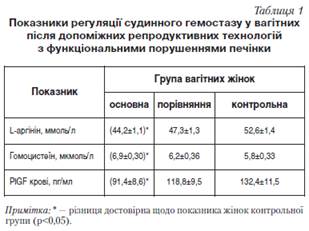
Результати дослідження та їх обговорення. За отриманими даними (табл. 1), у жінок основної групи спостерігалися суттєві зміни досліджуваних показників. Так, відмічалося достовірне щодо жінок контрольної групи зниження L-аргініну до 44,2±1,1 проти 52,6± 1,4 ммоль/л (p<0,05) та підвищення гомоцистеїну. При цьому виявлявся суттєво знижений рівень PlGF крові (91,4±8,6 проти 132,4±11,5 пг/мл у жінок контрольної групи, p<0,05), що засвідчило порушення процесів ангіогенезу, яке, своєю чергою, негативно впливало на розвиток і функціонування плаценти та обумовлювало виникнення ускладнень вагітності й порушення стану плода, які часто відмічались у жінок із гепатобіліарними змінами.
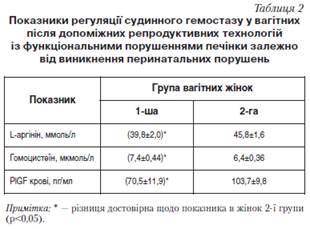
Для визначення ролі порушень регуляції судинного гомеостазу у виникненні ускладнень вагітності при печінкових порушеннях в основній групі виділено 2 підгрупи: 1-ша — 19 жінок із суттєвими акушерськими й перинатальними порушеннями (викидні та завмерлі вагітності, прееклампсія тяжкого ступеня, декомпенсований дистрес плода), 2-га — 31 жінка без таких порушень. Дослідженнями встановлено (табл. 2), що вагітність після програм ДРТ проходила з особливо тяжкими ускладненнями в тих жінок із гепатобіліарними порушеннями, в яких вже на початку вагітності формування і розвиток плаценти відбувались в умовах ендотеліальної дисфункції (зниження L-аргініну до 39,8±2,0 проти 45,8±1,6 ммоль/л у жінок без суттєвих порушень гестаційного процесу, p<0,05), негативної дії гомоцистеїну (підвищення до 7,4±0,44 проти 6,4±0,36 мкмоль/л, p<0,05), порушень процесів ангіогенезу (зниження PlGF крові 70,5± 11,9 проти 103,7±9,8 пг/мл, p<0,05). Отже, ці фактори можуть бути ранніми прогностичними маркерами тяжких акушерських і перинатальних порушень при індукованій вагітності в жінок із гепатобіліарними порушеннями.
Висновки. Вагітність після програм ДРТ проходить з особливо тяжкими ускладненнями в тих жінок із гепатобіліарними порушеннями, в яких вже на початку гестації формування й розвиток плаценти відбуваються в умовах ендотеліальної дисфункції (зниження рівня L-аргініну), негативної дії гомоцистеїну, порушень процесів ангіогенезу (зниження рівня PlGF крові), тобто ці фактори можуть бути ранніми прогностичними маркерами тяжких акушерських і перинатальних порушень при індукованій вагітності в жінок із гепатобіліарними порушеннями.
В умовах гомеостатичного дисбалансу в даної категорії жінок порушення ендотелію та факторів судинної регуляції лежать в основі патогенезу репродуктивних, акушерських і перинатальних ускладнень, що є теоретичною передумовою для розробки патогенетично спрямованого комплексу профілактики й лікування, спрямованого на корекцію виявлених порушень.
судинний порушення перинатальний вагітність.
Література
- 1. Бойчук О. Г Поліморфні варіанти гену ендотеліальної NO синтетази у жінок з безпліддям та порушеннями гепатобіліарної системи / О. Г Бойчук // Вісник Вінницького національного медичного університету. — 2015. — № 1 (Т. 19). — С. 74—77.
- 2. Дашкевич В. Е. Болезни печени и беременность / В. Е. Дашкевич // Неотложные состояния в акушерстве и гинекологии. — Київ: Здоров’я, 2000. — С. 249—258.
- 3. Ермолов С. Ю. Дисфункция эндотелия печеночных гемокапилляров: оценка и коррекция гемодинамики в терапии хронических заболеваний печени / С. Ю. Ермолов, В. Г Радченко, А. В. Шатров. — СанктПетербург, 2000. — 117 с.
- 4. Комиссарова Ю. В. Трубно-перитонеальное бесплодие: клиническое значение определения сосудисто-эндотелиального фактора роста в прогнозировании синдрома гиперстимуляции яичников / Ю. В. Комиссарова, Л. Н. Кузьмичев // Акушерство и гинекология. — 2010. — № 4. — С. 50—54.
- 5. Матякубова С. А. Коррекция дисфункции эндотелия у женщин группы риска развития гестационной гипертензии / С. А. Матякубова // Архивъ внутренней медицины. — 2015. — № 3. — С. 26—29.
- 6. Мурашко Л. Е. Содержание гомоцистеина, фолатов и витамина В12 в крови беременных с преэклампсией / Л. Е. Мурашко, Л. З. Файзуллин, Ф. С. Бадоева // Акушерство и гинекология. — 2012. — № 4. — С. 22—25.
- 7. Оценка состояния сосудистого эндотелия при различных акушерских патологиях / М. Пальцев, Л. Волкова, Е. Пальцева, О. Аляутдина // Врач. — 2011. — № 5. — С. 86—87.
- 8. Петрищев Н. Н. Дисфункция эндотелия. Причины, механизмы, фармакологическая коррекция / Н. Н. Петрищев. — Санкт-Петербург: ИИЦ ВМА, 2007. — 296 с.
- 9. Подольський В. В. Застосування сучасних допоміжних репродуктивних технологій та їх значення для вирішення питань репродуктивного здоров’я / В. В. Подольський, Н.І. Раковська, В. М. Бадюк // Здоровье женщины. — 2009. — № 40 (4). — С. 175—179.
- 10. Ратникова Л. И. Значение оксида азота в повреждении гепатоцитов при патологии печени / Л. И. Ратникова, И. В. Мельников // Эпидемиология и инфекционные болезни. — 2002. — № 4. — С. 50—54.
- 11. Романенко ТГ Профилактика преэклампсии у беременных с патологией печени / ТГ Романенко, ГН. Жалоба, О. В. Морозова // Здоровье женщины. — 2009. — № 3. — С. 74—76.
- 12. Рудакова Е. Б. Вспомогательные репродуктивные технологии. Проблемы потерь беременности / Е. Б. Рудакова, И. В. Бесман // Лечащий врач. — 2010. — № 3. — С. 46—48.
- 13. Decreased expressions of vascular endothelial growth factor and visfatin in the placental bed of pregnancies complicated by preeclampsia / S.C. Kim, J.K. Joo, D.S. Suh [et al.] // Journal of Obstetrics and Gynaecology Research. — 2012. — № 4 (38). — P 665—673.
- 14. Endothelial dysfunction after pregnancy-induced hypertension / A.C. Henriques, FH. Carvalho, H.N. Feitosa [et al.] // Int. J. Gynaecol. Obstet. — 2014. — № 3 (124). — P 230—234.
- 15. Hon W.M. Nitric oxide in liver diseases / W.M. Hon, W.H. Lee, H.E. Khoo // Annals of the New Jork Academy of sciences. — 2002. — Vol. 962. — С. 278—295.
- 16. Panther E. Liver diseases in pregnancy / E. Panther, H.E. Blum // Dtsch. Med. Wochenschr. — 2008. — № 133 (44). — Р 2283—2287.
Роль нарушений сосудистой регуляции в возникновении перинатальных осложнений у беременных высокого риска
В.В. Каминский, Т. В. Коломийченко, О. Г. Бойчук, Ю. О. Яроцкая, С. М. Корниенко Цель — установить роль нарушений сосудистой регуляции в возникновении перинатальных осложнений у беременных высокого риска.
Пациенты и методы. Обследованы 50 беременных женщин после вспомогательных репродуктивных технологий с гепатобилиарными нарушениями (основная группа) и 50 беременных женщин после вспомогательных репродуктивных технологий без таких нарушений (группа сравнения) и 50 соматически здоровых женщин с неиндуцированной беременностью (контрольная группа) в сроке беременности 14−16 недель.
Содержание L-аргинина в крови определяли с помощью фотометрического метода, в основу которого положена реакция L-нафтола с гипобромидным реактивом. Уровень гомоцистеина определялся методом ферментативной циклической реакции, с помощью набора Diasyis (Германия) с использованием анализатора «Respons 920» (Германия) по методике производителя. Для количественного определения плацентарного фактора роста человека (PLGF) в образцах плазмы крови использовался иммунохимический метод с электрохимиолюминисцентной детекцией (ECLIA). Результаты. Для определения роли нарушений регуляции сосудистого гомеостаза в возникновении осложнений беременности при печеночных нарушениях в основной группе выделено 2 подгруппы: 1-я — 19 женщин с существенными акушерскими и перинатальными нарушениями (выки-дыши и замершие беременности, преэклампсия тяжелой степени, декомпенсированный дистресс плода), 2-я — 31 женщина без таких нарушений. Установлено, что беременность после программ вспомогательных репродуктивных технологий проходила по особо тяжелыми осложнениями у женщин с гепатобилиарной патологией, у которых уже в начале беременности формирование и развитие плаценты происходили в условиях эндотелиальной дисфункции (снижение уровня L-аргинина до 39,8±2,0 против 45,8±1,6 ммоль/л у женщин без существенных нарушений геста-ционного процесса, p <0,05), негативного воздействия гомоцистеина (повышение до 7,4±0,44 против 6,4±0,36 мкмоль/л, p<0,05), нарушений про-цессов ангиогенеза (снижение уровня PIGF крови 70,5±11,9 против 103,7±9,8 пг/мл, p<0,05). Следовательно, эти факторы могут быть ранними прогностическими маркерами тяжелых акушерских и перинатальных нарушений при индуцированной беременности у женщин с гепатобилиарными расстройствами.
Выводы. В условиях гомеостатического дисбаланса у данной категории женщин нарушение эндотелия и факторов сосудистой регуляции лежат в основе патогенеза репродуктивных, акушерских и перинатальных осложнений, что является теоретической предпосылкой для разработки патоге-нетически обоснованного комплекса профилактики и лечения таких осложнений, направленного на коррекцию выявленных нарушений.
Ключевые слова: беременность, вспомогательные репродуктивные технологии, печень, акушерские осложнения, эндотелий.
Role of vascular regulation disturbances in the occurrence perinatal complications in high-risk pregnancies
V.V. Kaminsky, T.V. Kolomiychenko, O.G. Boychuk,.
Yu.O. Yarotskaya, S.M. Korniyenko, P.L. Shupik.
Purpose — to establish the role of disorders of vascular regulation in the occurrence of perinatal complications in pregnant women at high risk.
Patients and methods. The study included 50 pregnant women after ART with hepatobiliary disorders (study group) and 50 pregnant women after ART without such disorders (control group) and 50 somatically healthy women with non-induced pregnancy (control group) at 14−16 weeks of gestation. The content of L-arginine in the blood was determined by the photometric method, which was based on the L-naphthol with gipobromidnim reagent reaction. Homocysteine was determined by the enzymatic cycling reaction using a set Diasyis (Germany) using the analyzer «Respons 920» (Germany) in the manufacturer’s procedure. For the quantitative determination of human placental growth factor (PLGF) in samples of blood plasma used immunochemical electrochemistry fluorescent detection method (ECLIA).
Results. To determine the role of vascular homeostasis disorders regulation in the event of pregnancy complications in liver disorders in the study group allo-cated 2 groups: 1st — 19 women with essential obstetric and perinatal disorders (abortions and missed abortion, preeclampsia, severe, decompensated fetal distress), 2nd — 31 women without such disorders. It was found that pregnancy after ART programs held for particularly severe complications in women with hepatobiliary pathology, who already at the beginning of pregnancy, the formation and development of the placenta takes place under conditions of endothelial dysfunction (reduction of L-arginine to 39.8±2.0 versus 45.8±1.6 mmol/l in women without significant violations of gestation, p<0.05), the negative impact of homocysteine (an increase to 7.4±0.44 versus 6.4±0.36 mmol/l, p<0.05), violations of angiogenesis (PlGF decrease in blood to 70.5±11.9 versus 103.7±9.8 pg/ml, p<0.05). Consequently, these factors may be early prognostic markers of severe obstetric and perinatal disorders during induced pregnancy in women with hepatobiliary disorders.
Conclusions. In the context of homeostatic imbalance in this group of women violation of the endothelium and vascular regulation factors underlie the patho-genesis of reproductive, obstetric and perinatal complications, which is the theoretical precondition for the development of a pathogenetic substantiation of complex prevention and treatment of complications, aimed at correcting the violations.
Key words: pregnancy, ART, liver, obstetric complications, endothelium.
Сведения об авторах
Коньков Дмитрий Геннадьевич — д.мед.н., доц. каф. акушерства и гинекологии № 1 Винницкого НМУ им. Н. И. Пирогова. Адрес: г. Винница, ул. Пирогова, 56; тел. (0432) 57−03−60.
Булавенко Ольга Васильевна — д.мед.н., проф., зав. каф. акушерства и гинекологии № 2 Винницкого НМУ им. Н. И. Пирогова. Адрес: г. Винница, ул. Пирогова, 56; тел. (0432) 570 360.
Дудник Вероника Михайловна — д.мед.н., проф., зав. каф. педиатрии № 2 Винницкого НМУ им. Н. И. Пирогова. Адрес: г. Винница, ул. Пирогова, 56; тел. (0432) 570 360.
Буран Валентина Васильевна — к.мед.н., ассистент каф. акушерства и гинекологии № 1 Винницкого НМУ им. Н. И. Пирогова, зам. гл. врача Винницкого городского клинического родильного дома № 1 по поликлинической работе. Адрес: г. Винница, ул. Хмельницкое шоссе, 98; тел. (0432) 511 257.